Uno studio condotto dall’Istituto di genetica e biofisica “Adriano Buzzati-Traverso” del Cnr ha identificato le funzioni alterate causate da mutazioni nel gene ARX nella lissencefalia e nell’encefalopatia epilettica. La ricerca, realizzata con il supporto di Fondazione Telethon, è stata pubblicata su Human Molecular Genetics
Uno studio diretto da Maria Giuseppina Miano dell’Istituto di genetica e biofisica “Adriano Buzzati-Traverso” del Consiglio nazionale delle ricerche (Cnr-Igb), identifica le funzioni danneggiate in due gravi patologie neurologiche quali la lissencefalia e l’encefalopatia epilettica dello sviluppo, causate da mutazioni differenti del gene ARX il cui ruolo è fondamentale per il corretto sviluppo cerebrale. Lo studio è stato pubblicato sulla rivista Human Molecular Genetics ed eseguito in collaborazione con il Dipartimento di medicina molecolare e biotecnologie mediche dell’Università di Napoli “Federico II (Unina), il centro di ricerca e di diagnostica molecolare Ceinge-Biotecnologie Avanzate di Napoli e l’Istituto di bioscienze e biorisorse del Consiglio nazionale delle ricerche (Cnr-Ibbr), e con il sostegno di Fondazione Telethon.
Grazie a un approccio integrato che coniuga studi di proteomica con analisi in vivo, il gruppo di ricerca ha stabilito cosa avviene in presenza di una mutazione che abolisce o modifica le funzioni della proteina ARX. La ricerca, condotta in modelli animali mutanti, svela ciò che accade nelle cellule del cervello malato in conseguenza dell’una o l’altra mutazione, evidenziando contemporaneamente l’alterazione di numerosi processi funzionali, alcuni dei quali condivisi, altri strettamente dipendenti dal tipo di mutazione. “La grande quantità di dati ottenuti dall’indagine proteomica ha permesso di far luce sulle funzioni danneggiate in caso di lissencefalia o di encefalopatia epilettica”, spiega Denise Drongitis del Cnr-Igb e prima autrice dello studio. “A partire dall’anomala quantità di migliaia di proteine abbiamo definito i processi alterati in ciascuna condizione genetica analizzata”, aggiunge Marianna Caterino di Unina/Ceinge e altra prima autrice dello studio. “Grazie a studi di proteomica ed analisi in vivo, abbiamo scoperto che le mutazioni del gene ARX alterano funzioni molecolari e cellulari inaspettate – quali l’organizzazione del citoscheletro dei microtubuli, lo splicing alternativo dei geni Neurexina 1 e 2 e il controllo della sintesi proteica”, conclude Maria Giuseppina Miano del Cnr-Igb. “Abbiamo inoltre dimostrato come queste funzioni sono particolarmente danneggiate nei neuroni della corteccia stabilendo aspetti completamente nuovi della lissencefalia e dell’encefalopatia epilettica”. Questi risultati aiutano ulteriormente a capire la patogenesi di queste malattie e aprono a nuovi studi per identificare bersagli terapeutici e migliorare la condizione dei bambini con mutazioni ARX.
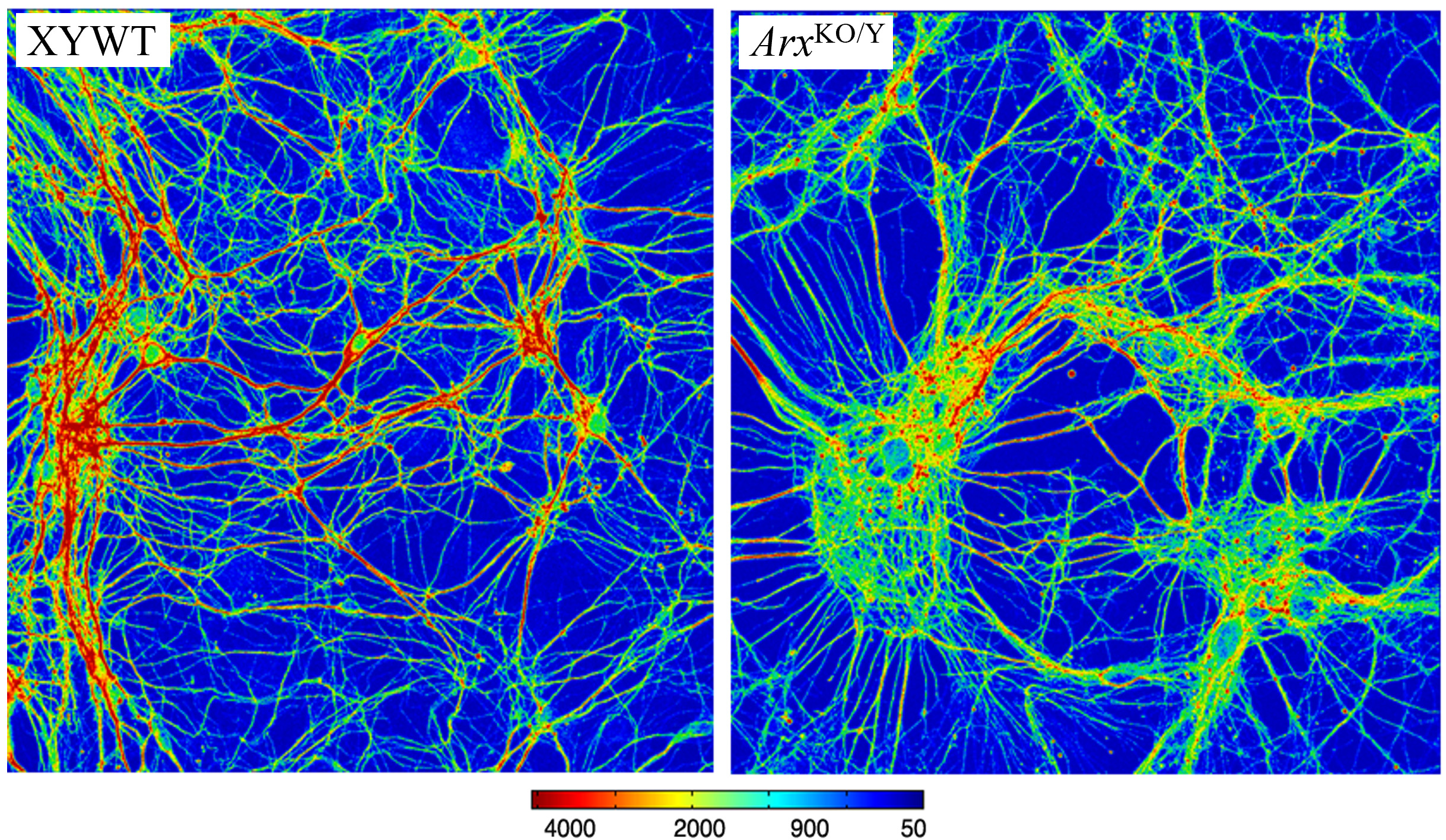
Immagine d’apertura: livelli di bIII-tubulina in neuroni murini isolati da corteccia normale (a sinistra) e corteccia malata (a destra). Da “Drongitis & Caterino” et al. 2022, Hum.Mol.Gen..